Jde rozpustit jen kousek molekuly?
Rozpustnost látky ve vodě a vodných roztocích je jednou ze základních vlastností, která určuje její dostupnost a použitelnost v biochemických i průmyslových aplikacích. K tématu přispěl Dr. Jan Heyda s kolegy z Pensylvánské Univerzity v čerstvě zveřejněné studii v Nature Chemistry.
Z každodenní zkušenosti v kuchyni očekáváme, že zvýšením teploty rozpustnost vzroste – cukr se dobře rozpouští v horkém čaji a sůl v horké vodě. Takového kofeinu rozpustíme v 1 litru vody cca 20 g při 25 °C, ale ve vroucí vodě je to už přes 600 g. Jenže pro málo rozpustné nepolární látky je to přesně naopak, takové oleje se při vyšší teplotě rozpouští méně. Obdobně můžeme v kádince ovlivňovat rozpustnost i výrazně složitějších molekul, například enzymů.
Buňky si ale nemohou dovolit používat změnu teploty k ovlivňování rozpustnosti, stability a funkce svých enzymů. Proto se v přírodě využívají jemnější mechanismy, například vystavení enzymu zvýšené koncentraci malých organických molekul či iontů. „Praha je s tématem rozpustnosti enzymů v osolených roztocích spojena déle než století. První systematickou studii totiž provedl profesor lékařské fakulty Franz Hofmeister už v roce 1888, kdy seřadil ionty podle jejich schopnosti vysolovat proteiny vaječného bílku. My jsme se zaměřili na thiokyanátový anion (SCN-), který rozpustnost zvyšuje," uvádí Dr. Heyda, jeden ze spoluautorů studie. Pražané si tuto řadu mohou prohlédnout na stěně 1. lékařské fakulty v ulici U Nemocnice.
Zkoumání vlivu iontů na rozpustnost i po více než sto letech přináší stále nová překvapení. Experimentálně teoretická spolupráce týmů z Pensylvánské Univerzity a VŠCHT Praha objevila paradoxní chování polyethylenoxidu, jehož rozpustnost je zvyšována thiokyanátanem sodným, zatímco rozpustnost jeho monomeru se účinkem té samé soli snižuje.
„Stěžejním pro úspěch publikované práce se ukázalo propojení simulace a dvou typů experimentu,“ podotýká Dr. Heyda. První sledoval, jak silně se váže thiokyanátový anion na každou jednotlivou monomerní jednotku [-CH2-CH2-O-]. Druhý změřil průměrnou strukturu vody v okolí molekuly polyethylenoxidu. Za pomoci počítačových simulací jsme tuto informaci zjemnili opět až na úroveň jednotlivých monomerních jednotek.
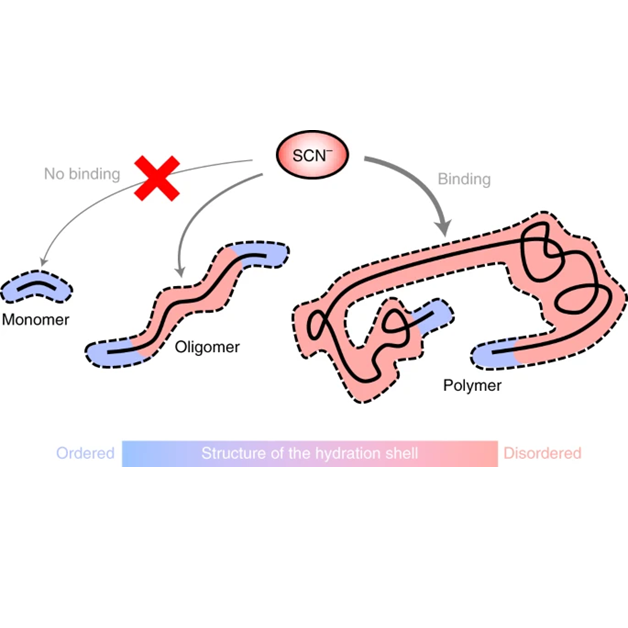
Jasně jsme přitom dokázali, že z míst s neporušenou hydratační strukturou (koncových skupin) je thiokyanátový anion vypuzován, zatímco k místům s porušenou strukturou vody vykazuje podstatnou vazbu. Toto chování je schématicky znázorněné na obrázku. Vysvětluje, proč thiokyanát sodný snižuje rozpustnost dimethoxyethanu (monomeru), slabě zvyšuje rozpustnost dimeru a silně zvyšuje rozpustnost delších polyethylenoxidů. Analogické chování jsme pozorovali i pro chemicky komplikovanější polymery na bázi akrylamidů, které jsou složením blízké peptidům.
Reference
Rogers, B.A., Okur, H.I., Yan, C. et al. Weakly hydrated anions bind to polymers but not monomers in aqueous solutions. Nat. Chem. (2021). https://doi.org/10.1038/s41557-021-00805-z







